Жидкие вещества


Средняя оценка: 4.2
Всего получено оценок: 529.
Средняя оценка: 4.2
Всего получено оценок: 529.
Соединение в агрегатном состоянии, занимающем промежуточное положение между твёрдым и газообразным состояниями, называется жидким веществом.
Строение
Молекулы жидкости не имеют строго упорядоченной структуры как в твёрдом веществе и могут перескакивать с одного места на другое, что объясняет текучесть жидкости. Расстояние между молекулами жидкого вещества близкое, но не такое большое, как между молекулами газов. Частицы жидкости не отрываются и не перемещаются свободно и хаотично.

Притяжение между молекулами достаточно сильное, чтобы сохранять межмолекулярное расстояние, но достаточно слабое, чтобы держать молекулы в статичном положении.
Жидкость держит объём, но не держит форму, совершая колебательные движения.
Физические свойства
Жидкость отличается от газов и твёрдых тел и имеет индивидуальные характеристики:
- текучесть – возможность принимать форму сосуда и двигаться под действием даже незначительной силы;
- вязкость – способность оказывать сопротивление перемещению одной части вещества относительно другой;
- малосжимаемость – невозможность уменьшить объём за счёт малого пространства между молекулами;
- смачивание – «прилипание» молекул жидкости к твёрдым телам;
- образование поверхностного натяжения – создание раздела фаз (жидкой и газообразной) в виде упругой мембраны.

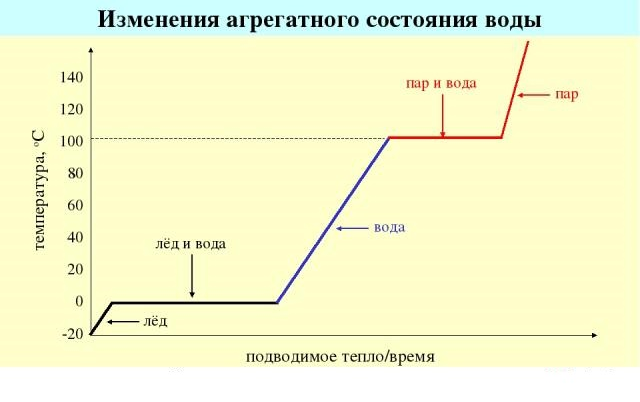
Жидкости могут существовать только в определённом интервале температур. При понижении температуры жидкость переходит в твёрдое состояние, при повышении – превращается в газообразное вещество. Границы температурного интервала зависят от давления.
Условно жидкости делят на две группы:
- чистые, состоящие только из молекул вещества;
- смеси, включающие дополнительные частицы и молекулы и других веществ.
Примерами жидких смесей являются кровь, морская вода, сок фруктов.
Многие жидкости органического и неорганического происхождения являются растворителями. Это вещества, способные разлагать (растворять) другие жидкие, твёрдые или газообразные вещества. К растворителям относятся этанол, спирт, ацетон, вода, аммиак.
В условиях невесомости жидкость приобретает форму капли за счёт поверхностного натяжения, создаваемого со всех сторон.
Классификация
Самая известная жидкость на планете – вода. Она характеризуется высокой текучестью, замерзанию при 0°C, испарению при 100°C. Вода не имеет высокой вязкости и является универсальным растворителем.
Однако существует множество других жидкостей, отличающихся от воды физико-химическими свойствами. Выделяют основные виды:
- атомарные, состоящие из атомов или сферических молекул (метан, аргон в виде жидкостей);
- двухатомные, состоящие из двух одинаковых атомов вещества (ртуть, жидкий водород, натрий);
- полярные, состоящие из полярных молекул (жидкий бромводород);
- ассоциированные, включающие водородные связи (вода, глицерин).
В физике отдельно выделяют квантовые жидкости и жидкие кристаллы.

Что мы узнали?
Из урока 11 класса узнали, что такое жидкости. Это текучие вязкие вещества, находящиеся между твёрдым и газообразным агрегатными состояниями. Жидкость принимает форму сосуда, но при этом имеет собственный объём. В жидком состоянии вещества находятся в определённом диапазоне температур. При смещении температуры жидкость переходит в твёрдое или газообразное состояние. Выделяют несколько видов жидкости в зависимости от их химического строения.
Тест по теме
- /5Вопрос 1 из 5
Чем характеризуется жидкость?